摘要:研制了猪脑心肌炎( EMCV )与猪圆环病毒(PCR-2 )二联灭活疫苗 EMCV/PCR-2 ,并选择小鼠和猪进行疫苗的安全性与免疫效力试验。结果显示: EMCV/PCR-2二联灭活疫苗对小鼠、仔猪、后备母猪和不同妊娠阶段母猪均安全。免疫小鼠时的最佳接种剂量为0.1mL ,首免和二免的保护率分别高达80%和100% ,免疫效果均高于相应单苗,并可产生各自的高水平抗体;免疫仔猪时的最佳接种剂量为2mL ,免疫效果略高于相应单苗和 PCV-2商品苗,且平均日增重最高,料肉比最低,攻毒保护试验结果表明可完全有效抵抗 EMCV 和 PCR-2强毒株的攻击。该疫苗为2种疾病的联合免疫提供了可能,达到“一针防两病”的效果,满足了 EMCV免疫的潜在需求。
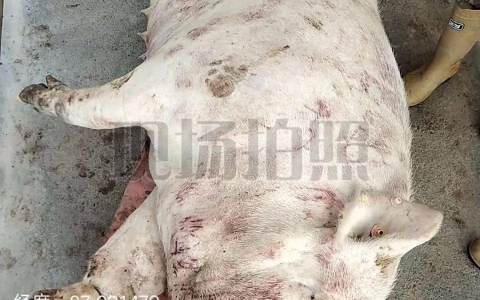
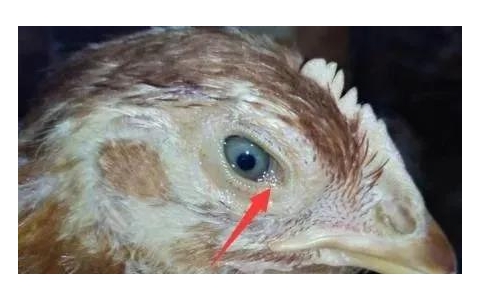
脑心肌炎( encephalomyocarditis,EMC)是由脑心肌炎病毒(encephalomyocarditis vrus , EMCV)引起的一种以脑炎、心肌炎和繁殖障碍为主要临诊特征的人兽共患传染病。自然条件下,EMCV 可感染家畜、啮齿类动物、野生动物以及灵长类动物,其中啮齿类动物是 其 自然 贮存 宿 主 和 主 要 传 播者,小鼠易感性极高,是最常用的实验动物模型,而感染最为广泛和危害最为严重的家畜是猪,可致使妊娠母猪发生流产、产死胎和弱仔,仔猪发生致死性心肌炎和脑炎等。近年来,通过病毒分离鉴定和血清学检测证实人感染发病也时有发生。猪圆环病毒病(porcine circovirus disease, PCVD)是由猪圆环病毒 2 型(porcine circovirus 2, PCR-2)引起的以仔猪断奶后全身衰竭综合征( PMWS )和猪皮炎肾病综合征( PDNS )为代表的多种疾病的总称,其临诊表现多样,主要特征为体质下降、消瘦、贫血、黄疸、生长发育不良、腹泻、呼吸困难、母猪繁殖障碍、内脏器官及皮肤广泛病理变化。此外,还可导致猪群产生严重的免疫抑制,从而导致继发或发生其他传染病。
EMCV 和 PCR-2 是当前国内猪场中感染率很高的2种重要的病原体,笔者前期研究已证明在养猪生产中二者混合或相互继发感染现象普遍存在,使得临床表现更为复杂,危害更为严重。使用安全高效的疫苗免疫易感猪则是防控 2 种疾病的最有效途径。 2010年以来,国内外已有多家商品化的PCR-2疫苗注册上市,疫苗类型主要为全病毒灭活苗和亚单位苗,临床大面积应用的结果证实这些疫苗均具有良好的免疫保护效果。国外早已成功研制出EMC灭活苗和弱毒活疫苗,近年来新型基因工 程 苗 的 研 发 也 获 得 较 大 进 展。而 EMCV/PCR-2二联灭活疫苗的研究尚未见报道,为了降低疫苗成本和免疫应激,简化免疫程序,本试验从生产实际出发,首次探索研制 EMCV/PCR-2二联灭活疫苗,并进行免疫效力试验,以评价其免疫保护性能。
1、材料与方法
1.1 病毒、细胞和试验动物
猪源 EMCV JZ1201株和 YM13 株均由本实验室分离、鉴定并保存,测定其 TCID 50 为 10 -9.66/0.1mL和 10 -8.51 /0.1mL,分别用于制备疫苗和攻毒保护试验。PCR-2河南流行株 HNYY由本实验室分离、鉴定并保存,生物学特性和免疫原性由高金良等做过相关研究,证实可作为 PCR-2疫苗候选株,经 SYBR Geen I实时荧光定量 PCR 方法测定病毒拷贝数为3.351×106Copies/μL ,用于制备疫苗。BHK-21传代细胞由本实验室保存, PK-15传代细胞由南京农业大学姜平教授惠赠。6周龄SPF级健康昆明小鼠由河南农业大学郑振宇教授惠赠,检测EMCV和PCR-2的ELISA抗体均为阴性。 3~4周龄健康仔猪由河南省丰源种猪场提供,8月龄后备母猪和不同妊娠阶段母猪由洛阳市鹅宿种猪场提供,检测EMCV 和PCR-2的ELISA 抗体均为阴性,在隔离条件下饲养。
1.2 主要试剂
RPMI-1640 、新生牛血清等购自美国 Hyclone公司;甲醛购自南通江天化学品有限公司;进口白油由辽宁益康生物制品有限公司提供;透析袋和聚乙二醇 20000 (PEG20000)分别购自上海索莱宝生物科技有限公司和上海研域生物科技有限公司; PCR-2 商品苗(LG 株)购自哈尔滨某公司。
1.3 EMCV 种毒培养条件的确定
将 JZ1201 株作连续10 倍稀释成 TCID50 分别为 10 -3.0 /0.1mL 、 10-4.0/0.1mL 、 10-5.0/0.1mL ,接种 BHK-21细胞培养至 16,20 , 24 , 30h 时测定病毒滴度,以确定最佳接种剂量。根据上述确定的最佳接种剂量,将JZ1201 株接种 BHK-21 细胞,感作漂洗后分别加入DMEM 维持液 4 , 6 , 8mL ,培养、收毒并测定病毒滴度,以确定最佳培养液用量。根据上述确定的最佳接种剂量和最佳培养液用量,将 JZ1201 株 BHK-21细胞,每隔4h取上清测定病毒滴度,以绘制EMCV的增殖曲线,并确定最佳收毒时间。
1.4 灭活疫苗制备
1.4.1 种 毒 灭 活 和 灭 活 效 果 检 验
向 制 备 的JZ1201 株 和HNYY 株 中 分 别 加 入 终 浓 度 为0.025%和0.3%的甲醛溶液,充分摇匀后,37 ℃灭活24h和48h ,期间每隔2~4h振摇1次,以使病毒液被充分灭活。随后吸取少量灭活后的2种疫苗毒,以1∶10稀释后分别接种于 BHK-21 细胞和PK-15细胞,盲传3代培养观察,均应无CPE出现,应用本实验室建立的 EMCV VP1 基因 RT-PCR 方法和PCR-2ORF - 2基因PCR方法检测结果均应为阴性。同时均设同批未经灭活的2种病毒液(1:10)作为对照。
1.4.2 病毒液浓缩
应用透析袋法进行浓缩。在透析袋上面均匀洒满 PEG20000,将 JZ1201 株和HNYY株分别加入、结扎,透析4~6h,收集浓缩后的病毒液,再用维持液平衡,使其变为原体积的50% 。
1.4.3 疫苗制备及检验
将灭活的JZ1201株和灭活并浓缩的HNYY 株,分别加入终浓度4%的吐温-80 ,充分混匀,即为单苗水相;将灭活并浓缩的JZ1201株和HNYY株,按照体积比1:1的比例混匀,加入终浓度4%的吐温-80,充分混匀,即为二联苗水相。按照参考文献的方法分别制成 EM-CV 灭活苗、 PCR-2灭活苗和 EMCV/PCR-2二联灭活苗,检测其物理性状并进行无菌检验。小鼠安全性试验中,选取6周龄 SPF 级健康昆明小鼠24只,随机分为3组,每种疫苗1组,将所制备的3种疫苗分别各皮下分点注射0.3mL ,连续观察14d ,同时设立对照 4 只,同等条件下饲养,详细记录各组小鼠的临床表现和注射部位变化。猪安全性试验中,将 3 种疫苗分别按一次单剂量接种安全性试验(2mL/头)、单剂量重复接种安全性试验(首免 2mL/头, 2 周后同等剂量二免)和一次超剂量接种安全性试验(4mL/头),分别经颈部肌肉注射 3 周龄健康仔猪各 8 头、 8 月龄后备母猪各 8 头和妊娠 30日龄、60 日龄、90 日龄母猪各 8 头,同时每组各设空白对照 4 头,同等条件下饲养。仔细观察试验猪的精神、食欲、生长速度、临床变化等,并测量体温(2次/日)至14d 。各组妊娠猪在同等条件下饲养至分娩,观察对繁殖性能及其所产仔猪的发育状况。
1.5 小鼠免疫效力检验
1.5.1 二联苗免疫剂量试验
将二联苗按 0.05 ,0.1 ,0.2mL 的剂量,分别免疫 6 周龄SPF级健康昆明小鼠各 10 只,同时设立空白对照,相同条件下隔离饲养,每周断尾采血,分离血清以检测 EMCV中和抗体。免疫后第 2 周,对每组的 5 只小鼠用YM13株以100LD50 腹腔接种攻毒。其余小鼠以首免时的同等剂量二免,继续每周断尾采血,分离血清以检测 EMCV 中 和 抗体,在 二 免 后 第 2 周 再 用YM13株以100LD50腹腔接种攻毒,记录小鼠存活数和死亡数。
1.5.2 小鼠免疫试验
将40只6周龄SPF级健康昆 明 小 鼠 随 机 分为 5 组,隔离饲养,分 别编为EMCV 灭 活 苗 组、 PCR-2 灭 活 苗 组、二 联 苗 组、PCR-2商品疫苗组和正常对照组。各组每只小鼠均皮下分点注射1.5.1确定的疫苗剂量,14d后同等剂量二免。分别于首免后1周采血,每周采1次至二免6周,分离血清用于检测EMCV中和抗体和PCR-2 ELISA抗体,并绘制抗体水平消长曲线。
1.6 仔猪免疫效力检验
1.6.1 二联苗免疫剂量试验
将二联苗按1 ,2 , 3mL 的剂量,分别经颈部肌肉注射免疫 3 周龄健康仔猪各 8 头, 2 周后以同等剂量二免。同时设立对照组,用生理盐水代替疫苗注射 3mL ,相同条件下隔离饲养。各组分别于免疫前、首免后第 2 周以及二免后第 2 、 4 周前腔静脉采血,分离血清测定 EM-CV 中和抗体和 PCR-2 ELISA 抗体,并绘制抗体水平动态曲线。各组于试验前称量平均初始重,整个试验期间每日仔细观察、记录试验猪的健康情况、采食量、日增重及饲料报酬,1个月后计算平均末重、平均日采食量、平均日增重及料肉比,以测定不同免疫剂量对仔猪生长性能的影响。
1.6.2 攻毒保护试验

56 头 4 周龄健康仔猪随机分为 7 组,隔离饲养,分别编为 EMCV 灭活苗组、PCR-2 灭活苗组、二联苗组、 PCR-2 商品疫苗组和 3个对照组。根据 1.6.1 确定的最佳剂量, 4 个试验组均肌肉注射相应疫苗,14d 后同等剂量二免。二免 2周后每组随机选取4头进行攻毒保护试验,具体操作见表1 ,其余4头饲养至二免4周试验结束。攻毒后每日测量体温,观察临床表现。
2、结果
2.1 EMCV种毒培养条件
2.1.1 最佳接种剂量和培养液最佳用量


JZ1201株在 TCID50 为10-4.0/0.1mL的接种剂量时病毒滴度最高,为最佳接种剂量(表2 )。用6mL培养液培养时的病毒滴度最高, TCID50 高达10-9.65/0.1mL(表3)。
2.1.2 增殖曲线测定和最佳收毒时间


JZ1201 株在接种 4~8h 时TCID50快速上升,12h 后上升变得缓慢,20h 时达到 10-9.51/0,.1mL , 24h 最高,为10-9.64/0.1mL ,随后开始逐步下降,据此可确定最佳收毒时间为接毒后 20~24h(表4)。其增殖曲线变化见图1 。
2.2 病毒液灭活效果检验



吸取少量灭活后的JZ1201株1:10稀释后,接种于 BHK-21细胞盲传3代无 CPE 出现,应用 RT-CPR 检测结果为阴性,对照组则产生明显 CPE ,RT-CPR 检测结果为阳性(图2、3 )。吸取少量灭活后的HNYY株1:10稀释后,接种于PK-15细胞盲传3代,应用PCR检测结果为阴性,对照组为阳性(图4 )。
2.3 疫苗检验
3种疫苗外观均为乳白色;冷水表面试验中,第1滴成云雾状扩散,以后各滴均不扩散;3000 r/min 离心15min均不破乳和分层;黏度检验结果均未超过5s 。无菌检验中均无杂菌生长。接种小鼠后,精神、食欲和体温无异常,注射部位未出现任何不良反应,吸收良好。一次单剂量接种安全性试验、单剂量重复接种安全性试验和一次超剂量接种安全性试验结果证明,试验组仔猪和8月龄后备母猪发育良好,体温、精神状态和食欲均正常,接种部位无任何不良反应,对照组也未见异常。试验组各阶段妊娠母猪均未出现繁殖障碍,在正常预产期范围内产出发育正常的健康仔猪,同条件下饲养的对照组妊娠母猪也无异常临床表现。
2.4 小鼠免疫效力检验
2.4.1 EMCV 中和抗体检测

各组在首免二联苗后,第1周内均未检测到中和抗体,第2周除0.05mL组外,其余2组已检测到中和抗体。二免后第1周各试验组抗体水平快速升高,但0.2mL组显著高于其他免疫组,第 2 周后差异更为显著(表 5、图4 )。
2.4.2 攻毒保护率及最小免疫剂量试验

按照Reed-Muench 法计算 PD50 。二联苗首免时的PD50( A)为 10-0.45头份,1个PD50 是0.35头份;二免时的PD50 ( B)为 10-0.55头份,1个PD50是0.28头份,表示该疫苗在首免和二免时分别接种0.35头份和0.28头份即可使 50% 小鼠获得保护(表 6 )。另外, 0.1mL 组首次免疫后保护率为 80% ,二免后保护率为100% ,说明注射 0.1mL 疫苗,无论是首免还是二免,均可获得高保护率,因此可确定为最佳接种剂量。
2.4.3 小鼠免疫试验



二联苗和 EMCV 灭活苗的EMCV 中和抗体消长曲线基本一致,均在首免2周时可测到,二免 2 周后快速升至峰值,随后逐步缓慢下降(图5),整体上二联苗的中和抗体水平要略高于EMCV 灭活苗(表7)。二联苗和 PCR-2灭活苗的PCR-2 ELISA抗体逐步上升(图6),二免1周时均已达到1:800 ,商品苗仅至 1:400;二联苗在二免 3周至最高值1:3200 ,显著高于其他2组,持续至二免 5 周时维持在1:1600,至二免 6 周时下降至 1:800 ,但仍高于PCR-2灭活苗和商品苗的1:400和1:200(表7)。
2.5 仔猪免疫效力检验
2.5.1 二联苗免疫剂量确定


二联苗不同剂量免疫后, EMCV 中和抗体增长曲线基本相似,均在首免2周时可检测到,二免2周后快速升高,至二免4周时维持高水平效价。 2mL组和3mL组差异不大,但都显著高于1mL组(表8 )。 PCR-2抗体同样在首免2周时均可在血清中检测到,但效价较低,二免2周后抗体水平快速升高,二免4周后仍可维持在高水平效价,2mL 组和3mL 组均高达1:3200(表8 )。对照组平均日增重为0.39kg ,料肉比为2.33 。2mL免疫组的平均日增重最高,为0.62kg,比1mL 免 疫 组、 3 mL 免 疫 组 和 对 照 组 分 别 增 加 了59.0% 、 24.0%和40.9% ,料肉比最低 (1.65),比1mL 免 疫 组、 3 mL 免 疫 组 和 对 照 组 分 别 降 低 了2.94% 、 21.05%和29.18%(表9)。
2.5.2 攻毒保护试验
EMCV 灭活苗组在整个攻毒期内试验猪未出现EMC的临床特征,攻毒后第1周体温均未超过39.5℃ ,第2周有2d 、第3周有1d体温超过39.5℃ ,随后全部恢复正常。对照组中的4头攻毒猪于攻毒后2~5d时出现体温升高(40~41℃ ),精神不佳,食欲减退和呼吸困难等症状,至试验结束无死亡,随机剖检2头,均可见心包有少量积液、脑部轻度充血等,其余未攻毒的4头猪在整个试验期内体温始终保持正常范围。PCR-2 灭活苗组和 PCR-2 商品苗组在整个攻毒期内试验猪均未出现 PCVD 的临床特征,攻毒后第 1 周体温均未超过 39.5 ℃,第2 周均有 2d 体温超过 39.5℃ ,第3周全部恢复正常。对照组的4头攻毒猪于攻毒后12d时开始出现体温升高(40℃左右),渐进性消瘦,皮肤苍白,腹股沟淋巴结肿大等,第16天死亡1头,其余至试验结束无死亡。随机剖检2头可见全身淋巴结水肿;间质性肺炎,呈棕黄色或棕红色斑驳状;心脏变形,质地柔软;肾肿胀,有灰白色坏死;脾肿大变形等。其余未攻毒的4头猪在整个试验期内体温始终保持正常范围。二联 苗 组 在 整 个 攻 毒 期 内 试 验 猪 均 未 出 现EMC和PCVD的临床特征,攻毒后第1周体温均未超过39.5℃ ,第3周有2d体温超过39.5 ℃ ,随后全部恢复正常。对照组的4头攻毒猪于攻毒1d时出现体温升高(41℃左右),精神极度沉郁,食欲废绝,呼吸困难,麻痹,7d时死亡3头,另1头存活至试验结束,但濒临死亡,剖检后均发现心肌严重变性,心包积液;脑部明显充血;脾肿大,并有锯齿样出血斑点;肾土黄色、有大面积灰白色坏死;全身淋巴结水肿等。其余未攻毒的4头猪在整个试验期内体温始终保持正常范围。
3、 讨论
优秀种毒的筛选和培育对于研发高效、安全的灭活 疫 苗 至 关 重 要。 本 试 验 选 用 TCID 50 高 达10-9.66/0.1 mL 的 良 种 猪 源 EMCV 河 南 流 行 株JZ1201进行优化培养条件,确定TCID 50为10-4.0/0.1mL 、 6mL培养液和接毒后20~24h分别是最佳接种剂量、最佳培养液用量和最佳收毒时间,从而为研制 EMCV 高效疫苗奠定了基础。
疫苗质量与有效抗原的含量密切相关。 PCR-2体外增殖能力较差,难以获得高毒价的病毒液而成为疫苗研发的主要瓶颈,病毒浓缩技术则不失为一种很好的选择,如苏金存将PCV-2细胞培养物通过中空纤维超滤膜组件浓缩10倍以上,使得抗原含量提高1个滴度。但迄今为止,将病毒浓缩技术应用于 EMCV 疫苗的研究尚未见报道。为保证足够的抗原含量,本试验尝试应用透析袋法对种病毒液进行 2 倍浓缩,研制出 EMCV/PCR-2 二联灭活疫苗。该疫苗免疫小鼠时的最佳接种剂量为 0.1mL ,首免和二免的保护率分别高达 80% 和 100% ,免疫效果均高于相应单苗,并可产生各自的高水平抗体,彼此间不存在相互干扰作用。免疫仔猪时的最佳接种剂量为 2mL ,二免4周后的 EMCV 中和抗体和PCR-2 ELISA 抗体均维持在高水平,整体上略高于相应单苗和 PCR-2商品苗,且平均日增重最高,料肉比最低,攻毒保护试验结果表明可完全有效抵抗EMCV 和PCR-2强毒株的攻击。值得注意的是,透析袋法是利用 PEG20000的高吸湿性吸收水分来进行浓缩,操作简便,但产量较低,浓缩过程缓慢,因此多用于试验性研究,在疫苗实际生产过程中可能需要利用大型浓缩装置,在 EMCV 上的浓缩效果是否良好,有待于进一步研究。
近年来,随着 PCR-2疫苗的大面积推广应用,使得该病的危害显著降低,猪场的免疫接种率逐年提高。但多年来, EMCV 在养猪生产中多表现为亚临床感染,实际危害性尚不突出,因而并未受到公共卫生界和兽医界的高度重视,尽管国外早已成功研制出 EMC 疫苗,但在生产中并未得到广泛推广应用。值得警惕的是,该病是一种具有自然疫源性的人兽共患疫病,对人类健康始终存在潜在的威胁,加之当前我国猪群中的EMCV 感染日益趋于严重,应加快高效疫苗的研制和推广。本试验所研制的 EM-CV /PCR-2二联灭活疫苗则为2种疾病的联合免疫提供了可能,免疫效果也优于各自单苗,在不需调整免疫程序,不需增加免疫应激和疫苗成本,可达到“一针防两病”的效果,满足了当前养猪生产中对EMCV免疫的潜在需求。